本報記者 張敏
日前,中國國家藥監局(NMPA)藥品審評中心(CDE)最新公示,傳奇生物旗下生物制品1類新藥西達基奧侖賽(cilta-cel,LCAR-B38M CAR-T細胞自體回輸制劑)擬納入突破性治療藥物名單。
“突破性治療”(breakthrough therapy designation)是中國國家藥監局(NMPA)不久前發布的《突破性治療藥物審評工作程序》文件的部分內容,旨在加速開發及審查治療嚴重的或威脅生命的疾病的新藥。
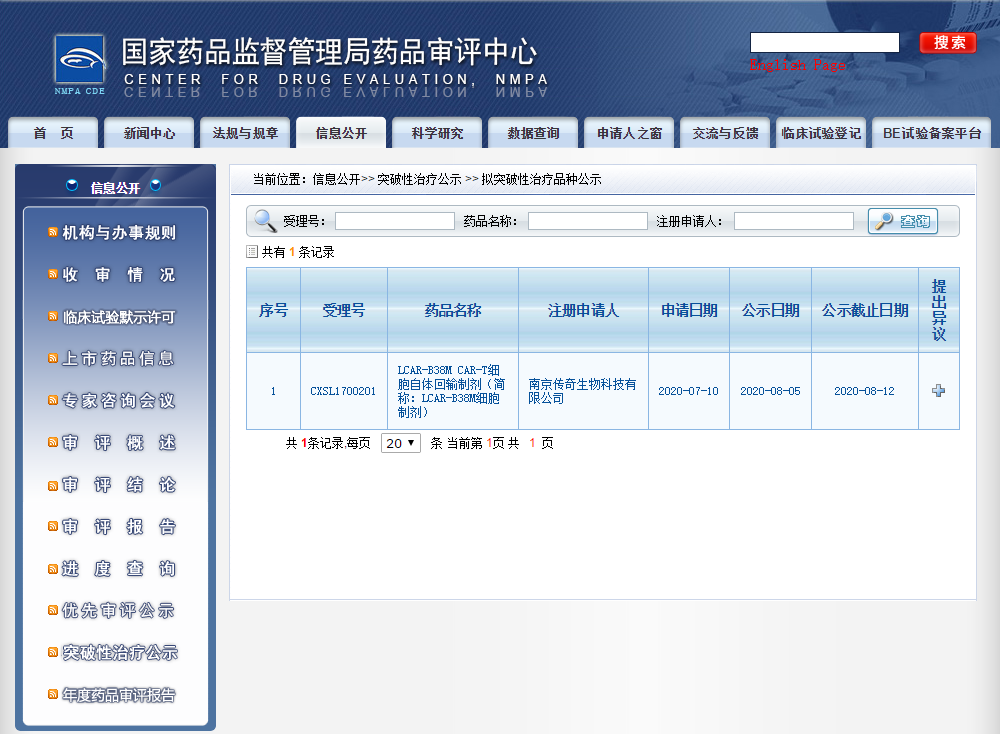
這是NMPA發布《突破性治療藥物審評工作程序》文件后,“突破性治療公示”專欄的首次更新,這也意味著這項特殊審評通道正式在中國啟動。
根據CDE公示信息,傳奇生物于今年7月10日為西達基奧侖賽申請了突破性治療,并于8月5日擬納入突破性治療品種名單。納入理由及依據為:符合《藥品注冊管理辦法》和《國家藥監局關于發布等三個文件的公告》(2020年第82號)有關要求,同意納入突破性治療藥物程序。公示日期截至8月12日。這是CDE“突破性治療公示”專欄首次更新。
突破性療法藥品審批有望提速
據記者了解,突破性療法的申請適用范圍為:藥物臨床試驗期間,用于防治嚴重危及生命或者嚴重影響生存質量的疾病且尚無有效防治手段或者與現有治療手段相比有足夠證據表明具有明顯臨床優勢的創新藥或者改良型新藥等,申請人可以在Ⅰ、Ⅱ期臨床試驗階段,通常不晚于Ⅲ期臨床試驗開展前申請適用突破性治療藥物程序。
對于獲得“突破性療法”認定的藥品而言,將縮短其漫長而昂貴的開發過程。這讓早期研究中顯示出良好前景的藥物盡快進入市場,而不必完成傳統的3個階段(Ⅰ~Ⅲ期臨床研究)的開發計劃。
此外,除了獲得快速審評通道,申請者還將獲得高效的審評員的指導。
西部證券此前發布的研報認為,突破性治療藥物認定規定對于重癥用藥和臨床優勢明顯的藥物通過突破性藥物認定后將得到藥審中心優先審評的資源傾斜。
在業內人士看來,中國突破性療法將會是未來一個重要的標簽,同樣會代表著中國的創新水平。中國突破性療法最重要的同樣是為了進一步加速具有臨床優勢藥物的中國上市進程;進一步滿足中國重大疾病的臨床治療需求。
CAR-T細胞療法有望加速獲批
記者了解到,西達基奧侖賽是由傳奇生物開發的一款靶向B細胞成熟抗原(BCMA)的CAR-T療法,作為一種結構新穎的CAR-T細胞療法,旨在增加其靶向癌細胞的綜合能力,用于既往接受過包括蛋白酶體抑制劑,免疫調節劑和抗CD38抗體的治療方案和在末次治療期間或之后出現疾病進展的復發或難治性多發性骨髓瘤(RRMM)成年患者。
強生(Johnson&Johnson)旗下楊森公司(Janssen)于2017年與傳奇生物達成戰略合作,在全球范圍內共同開發和推廣該在研創新療法。該產品于2018年獲得國家藥品監督管理局首個CAR-T臨床試驗申請(IND)批件,并與同年獲得美國FDA的IND批準。在獲此“突破性療法”之前,該產品已于2019年獲得歐洲藥品管理局優先藥物認定(PRIME)資格及美國FDA授予的突破性療法認定。
今年6月份,傳奇生物作為“中國CAR-T上市第一股”,在納斯達克掛牌交易,是2020年截至目前生物科技公司最大規模的IPO。據傳奇生物招股書顯示,西達基奧侖賽將于今年底前在美國提交上市申請,并于2021年在中國提交上市申請。
此次西達基奧侖賽擬納入突破性治療藥物名單,意味著這款產品有望加速獲批,早日為患者帶來新的治療選擇。
傳奇生物首席執行官章方良博士表示,國家藥品監督管理局藥品審評中心所推薦授予的突破性治療藥物認定,對于西達基奧侖賽治療中國的骨髓瘤患者的開發過程是一個重大的監管里程碑,傳奇和楊森將合作繼續致力在中國及全球推廣該試驗性療法。
(編輯 喬川川)
| 14:24 | 白銀有色2024年實現扣非凈利潤2.5... |
| 14:20 | 淘寶閃購閃現外賣大戰 最大力度補... |
| 14:19 | 京東互聯網醫院守護民眾五一健康出... |
| 14:19 | 深高速2025年第一季度扣非凈利潤同... |
| 14:17 | 容百科技發布2025年一季報 多業務... |
| 14:15 | 首創環保第一季度歸母凈利潤增長9.... |
| 14:09 | 股權落定 先鋒基金開啟新旅程 |
| 14:05 | 招商銀行:董事會決議公告 |
| 14:05 | 恒順醋業:第九屆董事會第十次會議... |
| 14:05 | 金隅集團:第七屆監事會第四次會議... |
| 14:05 | 百龍創園:第三屆董事會第十五次會... |
| 14:05 | 空港股份:第八屆董事會第八次會議... |
版權所有證券日報網
互聯網新聞信息服務許可證 10120180014增值電信業務經營許可證B2-20181903
 京公網安備 11010202007567號京ICP備17054264號
京公網安備 11010202007567號京ICP備17054264號
證券日報網所載文章、數據僅供參考,使用前務請仔細閱讀法律申明,風險自負。
證券日報社電話:010-83251700網站電話:010-83251800 網站傳真:010-83251801電子郵件:[email protected]

掃一掃,即可下載

掃一掃,加關注

掃一掃,加關注